Опыт лечения пациентов с доброкачественной гиперплазией предстательной железы и дефицитом тестостерона в амбулаторной практике
Камалов А.А., Василевский Р.П., Охоботов Д.А.
Сведения об авторах:
- Камалов А.А. – академик РАН, д.м.н., профессор, директор МНОЦ МГУ им. М.В. Ломоносова, заведующий кафедрой урологии и андрологии ФФМ МГУ им. М.В. Ломоносова, AuthorID 759356
- Охоботов Д.А. – к.м.н., ст. науч. сотр. научного отдела «Урологии и андрологии» МНОЦ МГУ им. М.В. Ломоносова, AuthorID 759176
- Василевский Р.П. – врач-уролог ГБУЗ «ГП № 134 ДЗМ», AuthorID 1031392
DOI: 10.29188/2222-8543-2020-12-2-112-116
ВВЕДЕНИЕ
Половые гормоны оказывают ключевое влияние на системный метаболизм. Среди мужчин в возрасте от 40 до 79 лет распространенность биохимического андрогенодефицита и клинически выраженного дефицита тестостерона достигает 2,1–5,7%. Причем частота низкого уровня тестостерона без значимых клинических симптомов в этой же возрастной группе составляет 12,8% [1]. Наиболее часто у мужчин с дефицитом тестостерона наблюдаются: ухудшение либидо, нарушение эректильной и эякуляторной функции, повышенная усталость и снижение настроения [2,3]. Серьезными сопутствующими состояниями, на которые следует обращать внимание при диагностике дефицита тестостерона, являются метаболический синдром, ожирение, сахарный диабет второго типа, иные обменные заболевания, течение которых может изменять концентрацию тестостерона в организме [4,5]. Важно знать, что прием таких препаратов, как группа опиоидов, группа статинов, антагонисты рецепторов к дофамину, группа стероидов, блокаторы 5-α-редуктазы, значимо меняют уровень тестостерона [6,7]. Привычные интоксикации такими веществами, как каннабиноиды, алкоголь, иные наркотические средства, могут изменять содержание тестостерона в организме [8,9]. Назначение лекарственных форм тестостерона необходимо больным с признаками его возрастного дефицита, который сопровождается ухудшением течения сопутствующих заболеваний.
Целью настоящей работы стало определение влияния дополнительной терапии трансдермальной формой препарата тестостерона в сочетании с классической терапией доброкачественной гиперплазии предстательной железы (ДГПЖ) альфа-адреноблокаторами (α-АБ). В исследовании представлены данные проведенной терапии ДГПЖ как в моно-режиме α-адреноблокаторами, так и сочетанной терапии (α-адреноблокаторами в комбинации с тестостероном в форме геля).
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Формирование исследуемой группы происходило с III.2013 г. по IX.2017 г. в ходе общего поликлинического приема в кабинете уролога ГБУЗ «Городская поликлиника № 134 ДЗМ». В рамках установленного дизайна исследования были разработаны критерии включения и исключения.
Критерии включения: возраст 49-70 лет, объем предстательной железы больше 40 см3 , содержание общего тестостерона меньше 12,1 нмоль/л, максимальная скорость потока мочи (Qmax) меньше 15 мл/с. Критерии исключения: содержание простатоспецифического антигена (ПСАобщ) больше 4 нг/мл, применение препаратов групп ингибиторов 5-α-редуктазы (5-АРИ) и α-АБ в течение последних 12 месяцев, другие официальные противопоказания для назначения препаратов тестостерона.
Из всего пула пациентов (521 человек), принятых урологом нашей медицинской организации в течение выше означенного периода времени, 184 мужчины подошли под критерии включения. 60 человек подписали соответствующую форму информирования, согласившись таким образом на участие в исследовании. Вошедшие в исследование мужчины имели дефицит тестостерона и ДГПЖ. Все пациенты были разделены на две группы по тридцать человек в каждой.
В первой (I) группе больные получали в моно-режиме селективный α-АБ (8 мг/сут). Пациенты второй (II) группы получали сочетанную терапию, включавшую трансдермальный препарат тестостерона в форме геля по 5 г/сут. Весь курс терапии в обеих группах составил полгода.
Диагностический процесс проводился перед началом терапии и во время визитов к врачу через каждые два месяца в установленном объеме в течение полугода (всего четыре визита). Диагностический комплекс включал в себя сбор жалоб пациентов и анамнестических данных, физикальное обследование с определением массы тела и окружности талии; вычисление индекса массы тела (ИМТ), заполнение шкалы IPSS (Международная система суммарной оценки заболеваний предстательной железы, International Prostate Symptom Scorе) с индексом QoL (индекс оценки качества жизни) и опросника МИЭФ-5 (Международный индекс эректильной функции), определение уровня общего тестостерона, общего уровня специфического антигена предстательной железы (ПСАобщ), урофлоуметрию (УФМ), трансректальное ультразвуковое исследование предстательной железы (ТРУЗИ), определение объема остаточной мочи. При очередной плановой встрече с урологом всем пациентам давались устные и письменные рекомендации по усилению физической активности и изменению пищевого поведения. Общая характеристика больных представлена в таблице 1.
Таблица 1. Обобщенная характеристика пациентов двух групп
Table 1. Generalized characteristics of patients in two groups
| Показатель indicator |
Значение value |
Норма norm |
|---|---|---|
| Масса тела, кг weight, kg |
107,6 [95,5; 123] | |
| Возраст, в годах Age, in years |
53 [46; 59] | |
| Окружность талии (ОТ), см Waist circumference, cm* |
115 [110; 125] | ≤ 93 |
| Индекс массы тела (ИМТ), кг/м2 Body mass index (BMI), kg / m2 |
34,41 [30,22; 39,8] | До 25 |
| Уровень тестостерона общего, нмоль/л Total testosterone, nmol/l |
7,6 [5,5; 9,8] | 12–33 |
| Уровень тестостерона свободного, пкмоль/л Testosterone free, pmol/l |
147,6 [107,6; 187,8] | > 243 |
| Уровень глобулина, связывающего половые гормоны, нмоль/л Sex-binding globulin Hormones (SHBG), nmol/l |
33 [24,2; 43,7] | 10–57 |
| Уровень холестерина общего, ммоль/л Total cholesterol, mmol/l |
4,8 [4,1; 5,2] | 3,3–5,2 |
| Уровень глюкозы крови, ммоль/л Blood glucose, mmol/l |
4,7 [4,2; 5,1] | 4–6,1 |
| Уровень гематокрита, % Hematocrit, % |
45 [43,5; 48] | 42–48 |
| Уровень простатоспецифического антигена общего (ПСАобщ), нг/мл PSAtotal, ng/ml |
2,4 [1,6; 2,9] | 0–4 |
| Объем предстательной железы, см3 Prostate volume, cm3* |
58,4 [51,8; 67,9] | < 25 |
| Qmax, мл/с (урофлоуметрия) Qmax, ml / s* (uroflowmetry) |
12,3 [9,8; 15,6] | ≥ 15 |
| -PSS / Qol, баллы I-PSS / Qol, points* (questionnaires) | 25/4 [21/3; 29/5] | < 7 |
Примечание: достоверные изменения в ходе периода наблюдения *р<0,05 (парный t-критерий)
Note: significant changes during the observation period * p<0.05 (paired t-test)
Проведен статистический анализ данных, извлеченных из регистрационных карт больных. Выполнена обработка полученного материала на персональном компьютере с использованием пакета стандартных прикладных программ Stаtistiса Biоstаtv. 6.3., Мiсrоsоft Officе Ехcеl 2007, SРSS.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Абсолютно все пациенты завершили обследование. Окончательные результаты лечения пациентов с дефицитом тестостерона и ДГПЖ по обеим группам отражены в таблице 2. Анализ некоторых показателей (холестерин, глюкоза) не был помещен в результаты исследования в связи с малоинформативной практической значимостью в отношении заболеваний предстательной железы (ПЖ). В I группе отмечено статистически достоверное уменьшение объема остаточной мочи (с 78 до 18 мл), увеличесние максимальной объемной скорости потока мочи (с 11 до 18 мл/сек), уменьшение сумарного количества баллов по шкале I-PSS (c 25 до 15 баллов), увеличение баллов по шкале МИЭФ (с 5,3 до 7,1). Во 2 группе эти же показатели изменялись больше: объем остаточной мочи уменьшился с 72 до 19, Qmax – увеличилось с 13,3 до 21,1, сумма баллов по шкале IPSS уменьшилась с 25 до 8,9, сумма баллов по шкале МИЭФ увеличилась с 6,3 до 26,6 баллов.
Таблица 2. Сравнительная динамика результатов терапии пациентов с дефицитом тестостерона и ДГПЖ в обеих группах
Table 2. Comparative dynamics of therapy results in patients with testosterone and BPH deficiency in both groups
| Показатель indicator |
I группа I group |
II группа II group |
||
|---|---|---|---|---|
| До терапии before therapy |
После терапии after therapy |
До терапии before therapy |
После терапии after therapy |
|
| Окружность талии (ОТ), см Waist circumference, cm* |
114 | 110 | 116 | 103,2 |
| Тестостерон общий, нмоль/л Total testosterone, nmol/l |
7,5 | 7,5 | 7,8 | 18,2 |
| Простатоспецифический антиген общий (ПСАобщ), нг/мл PSAtotal, ng/ml |
2,41 | 2,35 (р <0,01) | 2,24 | 1,8 (р <0,01) |
| Объем предстательной железы, см3 Prostate volume, cm3* |
53,3 | 53,7 | 55,0 | 61,2 |
| Объем остаточной мочи , мл* Residual urine volume, ml* |
78 | 18 | 72 | 19 |
| Qmax, мл/с (урофлоуметрия) Qmax, ml / s* (uroflowmetry) |
11 | 18 | 13,3 | 21,1 |
| IPSS / Qol, баллы I-PSS / Qol, points* (questionnaires) | 25/4,9 | 15,1/2,8 | 25/4,2 | 8,9/2,6 |
| МИЭФ, баллы* ICEF, points* (questionnaire) | 5,3 | 7,1 | 6,3 | 26,8 |
| Индекс массы тела (ИМТ), кг/м2 Body mass index (BMI), kg / m2 | 33,1 | 30,0 | 35,3 | 27,1 |
| Глюкоза крови, ммоль/л Blood glucose, mmol/l | 4,6 | 4,5 | 4,8 | 4,4 |
| Холестерин общий, ммоль/л Total cholesterol, mmol/l | 4,7 | 5,1 | 5,2 | 4,6 |
Примечание: достоверные изменения в ходе периода наблюдения *р<0,05 (парный t-критерий)
Note: significant changes during the observation period * p<0.05 (paired t-test)
Необходимо отдельно продемонстрировать изменения показателей ПСАобщ. Отмечено, что к концу третьего месяца данного исследования уровень ПСАобщ во II группе пациентов снизился. При этом в I группе существенных изменений по данному параметру не установлено. В целом, уровень ПСАобщ в группе монотерапии (I) уменьшился на 20 % (рис. 1). Лишь только на 3-м и 4-м визитах определены статистически значимые отличия между группами по данному критерию.
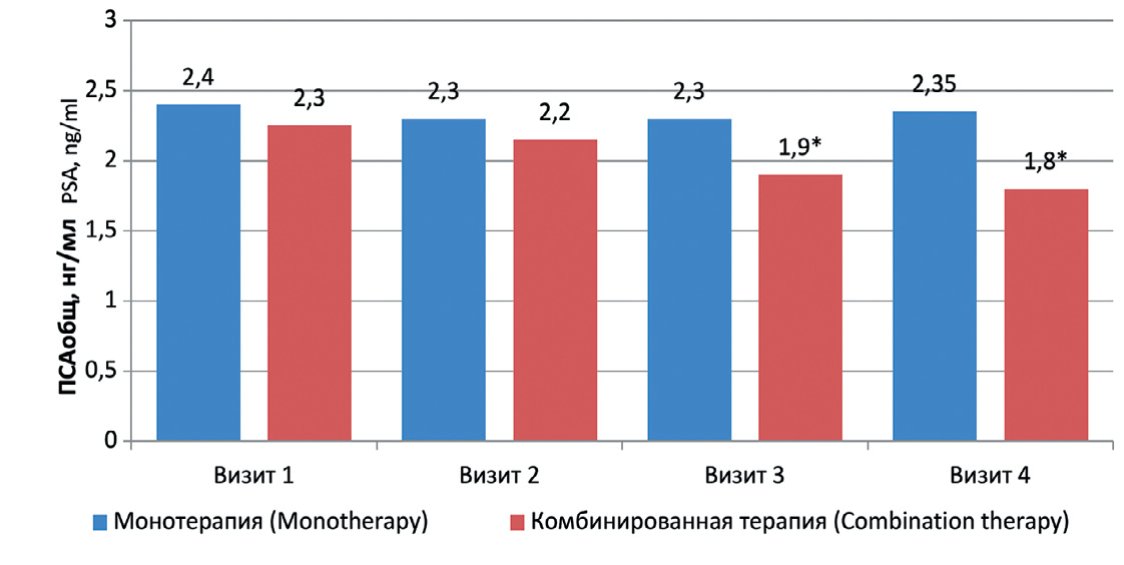
Рис. 1. Сравнительная динамика уровней ПСАобщ в двух группах наблюдения
Fig. 1. Comparative dynamics of PSA levels was observed in two observation groups. * р = 0,01
В отношении изменений объема предстательной железы необходимо сказать, что итоги терапии пациентов с дефицитом тестостерона и ДГПЖ в двух группах стали весьма ожидаемыми. В I группе значимых изменений не последовало. Во II группе, наоборот, установлено небольшое увеличение объема ПЖ в среднем на 6,2 см3 (на 11,3%), что явилось статистически недостоверным (рис. 2).
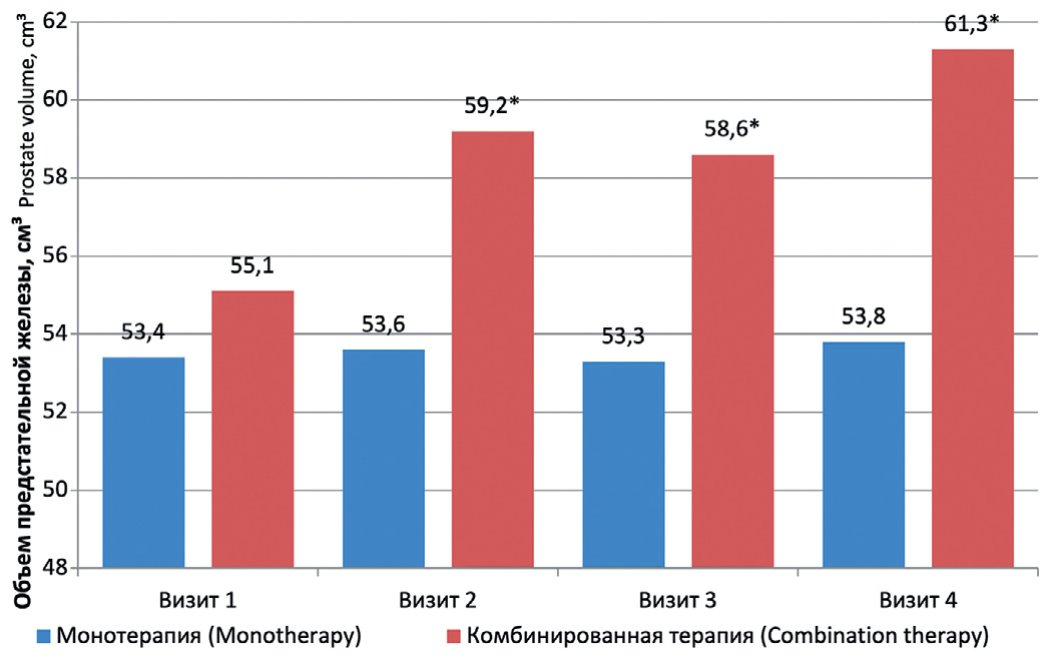
Рис. 2. Сравнительная динамика показателя объема предстательной железы (см3) в течение всего исследования
Fig. 2. Comparative dynamics of the prostate volume index (cm3) during the entire study
Результаты исследования уродинамики говорят о повышении максимальной скорости мочеиспускания у больных обеих групп (рис. 3). К четвертому визиту во II группе параметр составил 22 мл/с; (изначально=13 мл/с) р=0,05, а у пациентов I группы – 18 мл/с; (изначально = 11 мл/с) р=0,05 .
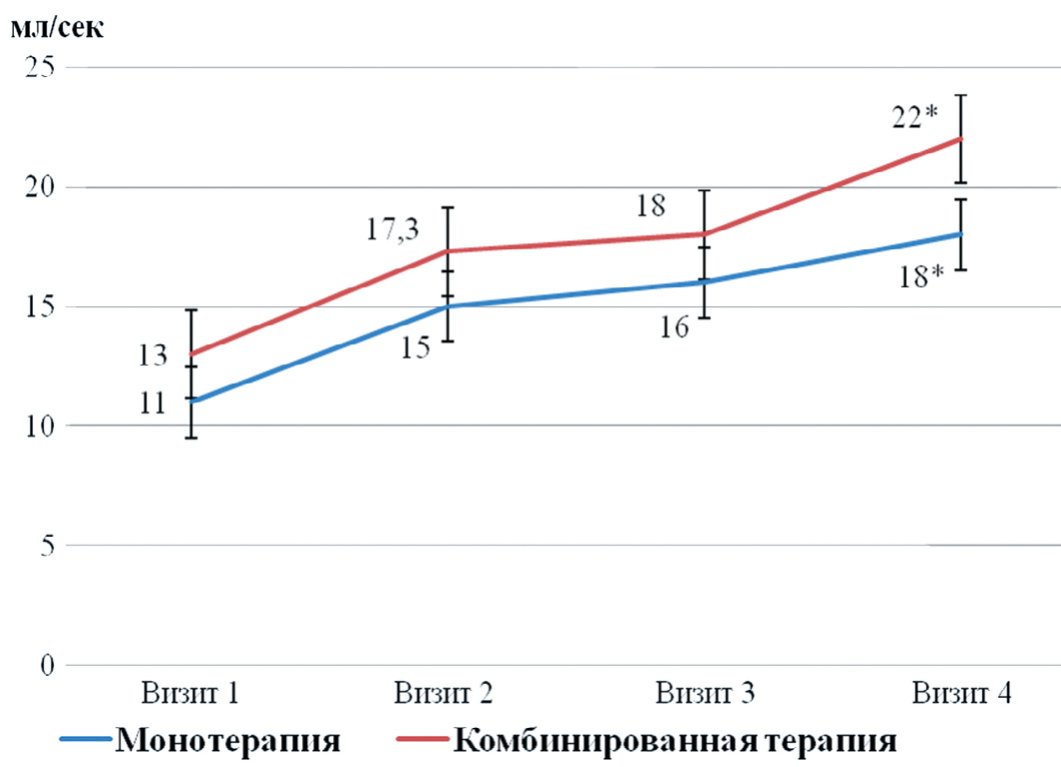
Рис. 3. Сравнительная динамика показателя Qmax в двух группах наблюдения
Fig. 3. Comparative dynamics of the Qmax indicator in two observation groups *р < 0,05 нмоль/nmol
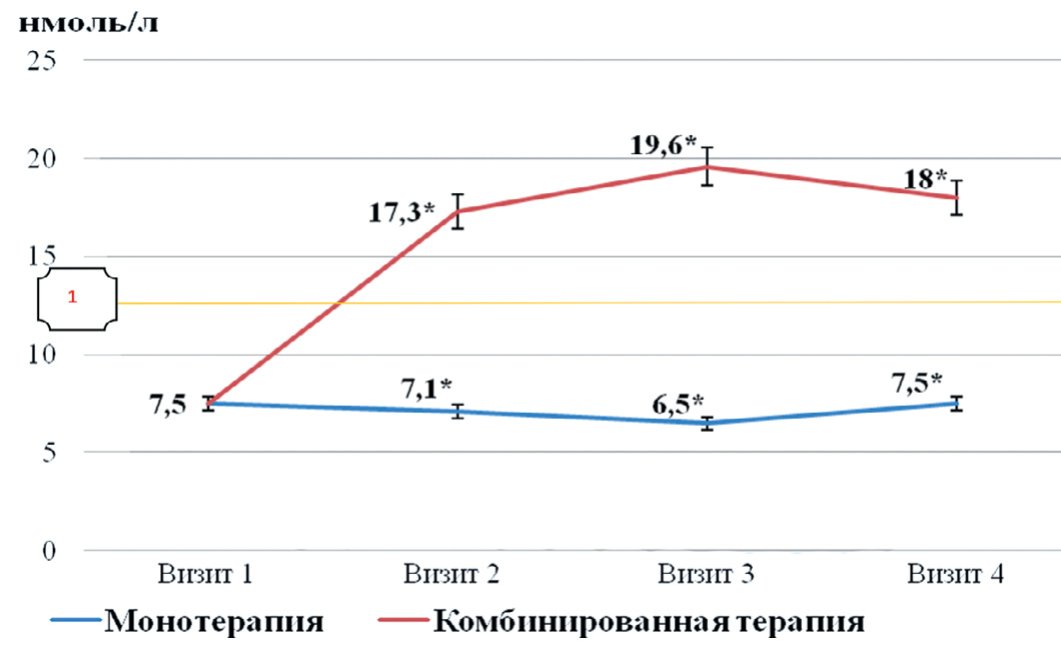
Рис. 4. Сравнительная динамика уровня общего тестостерона в двух группах наблюдения
Fig. 4. Comparative dynamics of the level of total testosterone in two observation groups *р < 0,05
Анализ изменения уровня общего тестостерона показывает следующее. Во II группе получено увеличение и нормализация содержания общего тестостерона (с 7,5 до 18 нмоль/л; р=0,05). Таким образом, он стал в 2,2 раза выше, чем в I группе, где желаемых изменений не было зафиксировано (рис. 4).
Сопоставление изменений окружности талии показало, что во II группе к завершению лечения в отношении этого показателя изменение оказалось на 8 % эффективнее, чем в I группе (рис. 5).
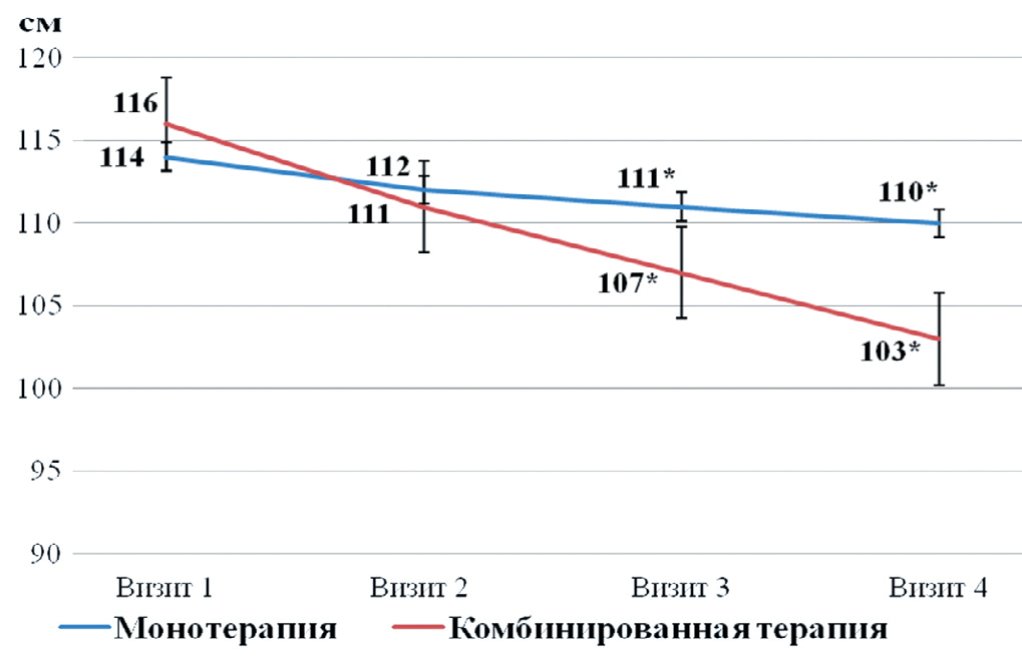
Рис. 5. Сравнительная динамика изменений окружности талии в двух группах наблюдения
Fig. 5. Comparative dynamics of changes in waist circumference in two observation groups *р < 0,05
ОБСУЖДЕНИЕ
Известен факт, что у мужчин органы урогенитальной системы во многом имеют андрогенно-рецепторную зависимость. Поэтому дефицитом тестостерона объясняется развитие пагубных влияний на функциональное состояние данной сферы, что патогенетически обосновано. Необходимо четкое понимание того, что ДГПЖ – это не изолированная урологическая патология, а очевидная системная проблема, в основе которой лежат общие возраст-ассоциированные гормонально-метаболическими нарушения. На наш взгляд, предвидеть и в определенной степени предупредить развитие ДГПЖ возможно за счет своевременной диагностики и рационального восполнения гормональных дефицитов. Назначение комбинированной терапии у пациентов с ДГПЖ на фоне возрастного дефицита тестостерона приводит к улучшению результатов терапии основного заболевания. В частности, приводит к уменьшению баллов по шкале IPSS на 24,5%, повышением QoL в среднем на 0,87 балла. Несмотря на то, что на фоне комбинированной терапии получено увеличение объема ПЖ (в среднем на 11,3%), клинические проявления ДГПЖ компенсируются более высокой скоростью мочеиспускания. На фоне коррекции сопутствующего дефицита тестостерона было отмечено повышение качества жизни пациентов, увеличение баллов по шкале МИЭФ (в среднем на 4,85 балла), уменьшение веса и окружности талии (на 8% по сравнению с контролем), что положительно сказывается на общем самочувствии пациентов. Положительную динамику в обеих группах в части некоторых антропометрических показателей (вес, ИМТ), скорее всего, следует трактовать так, что мужчинам двух групп выдавались одинаковые рекомендации по ЗОЖ (правильное питание, фитнес, жизнь без пагубных привычек и т.д.). Незначительное и статистически недостоверное повышение общего ПСА может быть объяснено увеличением объема предстательной железы. Но так как клиническое течение ДГПЖ в группе II улучшилось более заметно, назначение трансдермальной гелевой формы тестостерона в целом себя оправдывает.
Итоги представленного исследования соответствуют зарубежным работам, что делает возможным их применение в рутинной практической работе [7,8,10]. Однако, невзирая на достаточное число работ, посвященных изучению влияния дефицита тестостерона на качество мочеиспускания, до настоящего момента окончательно неясна патофизиологическая основа этих состояний. Считается, что гипогонадизм – одно из самых ранних проявлений метаболического синдрома. В большом количестве исследований доказана связь стойкого дефицита тестостерона с симптомами нижних мочевых путей [7,8]. Предметное воздействие тестостерона на ПЖ тоже служит основанием для глубоких размышлений. Принято полагать, что тестостерон – инициатор увеличения ПЖ. Однако, имеется весомое количество опубликованных исследований, в которых доподлинно не показана корреляция между уровнем тестостерона и темпами роста ПЖ. В связи с чем данный вопрос остается дискутабельным. Взаимосвязь между насыщением организма тестостероном, формированием метаболического синдрома и прогрессированием СНМП – может функционировать по принципу взаимного отягощения.
ЗАКЛЮЧЕНИЕ
Проведенное исследование демонстрирует, что заместительная гормональная терапия препаратами тестостерона у больных с ДГПЖ абсолютно безопасна и объективно ведет к улучшению качества их жизни (и не только в контексте урологии). Комбинированная терапия ДГПЖ и возрастного дефицита тестостерона способствует улучшению клинических результатов течения основного урологического заболевания и повышению качества жизни пациентов, для которых сексуальная активность является актуальной.
ЛИТЕРАТУРА
- Ефремов Е.А., Красняк С.С. Возможные риски при терапии тестостероном. Экспериментальная и клиническая урология 2017;(1):90-97. [Efremov E.A., Krasnyak S.S. Possible risks with testosterone therapy. Eksperimental’naya i klinicheskaya urologiya = Experimental and Clinical Urology 2017;(1):90-97. (In Russian)].
- Мамедов М.Н., Шарвадзе Г.Г., Поддубская Е.А., Салек Б.Г., Мехтиевз Т.В., Мехтиев С.Х. Междисциплинированный подход к проблемам мужского здоровья с целью улучшения качества и продолжительности жизни. Профилактическая Медицина 2011;14(5):30-35. [Mamedov M.N., SHarvadze G.G., Poddubskaya E.A., Salek B.G., Mekhtievz T.V., Mekhtiev S.H. An interdisciplinary approach to men’s health in order to improve quality and longevity. Profilakticheskaya Medicina = Preventive Medicine 2011;14(5):30-35. (In Russian)].
- Baillargeon J, Urban RJ, Kuo YF, Holmes HM, Raji MA, Morgentaler A, et al. Screening and Monitoring in Men Prescribed Testosterone Therapy in the U.S., 2001–2010. Public Health Rep 2015;130(2):143-52. doi: 10.1177/003335491513000207
- Basaria S. Male hypogonadism. Lancet 2014;383(9924):1250-63. doi: 10.1016/S0140-6736(13)61126-5. Epub 2013 Oct 10.
- Mulhall JP, Trost LW, Brannigan RE, Kurtz EG, Redmon JB, Chiles KA, et al. Evaluation and Management of Testosterone Deficiency: AUA Guideline. J Urol 2018 Aug;200(2):423-432. doi: 10.1016/j.juro.2018.03.115. Epub 2018 Mar 28
- Herati AS, Kohn TP, Butler PR, Lipshultz L. Effects of Testosterone on Benign and Malignant Conditions of the Prostate. Curr Sex Health Rep 2017 Jun; 9(2):65-73. doi: 10.1007/s11930-017-0104-7. Epub 2017 Apr 26.
- Ko IG, Hwang L, Jin JJ, Kim SH, Han JH, Jeon JW, et al. Add-on Therapy With the α-Blockers Tamsulosin and Naftopidil Improves Voiding Function by Enhancing Neuronal Activity in Prostatic Hyperplasia Rats. Int Neurourol J 2018 Mar;22(1):20-29. doi: 10.5213/inj.1836064.032. Epub 2018 Mar 31.
- Lee JH, Kim Y, Park YW, Lee DG. Relationship between benign prostatic hyperplasia/lower urinary tract symptoms and total serum testosterone level in healthy middle-aged eugonadal men. J Sex Med 2014 May;11(5):1309-1315. doi: 10.1111/jsm.12489. Epub 2014 Feb 24.
- Jarvis TR, Chughtai B, Kaplan SA. Testosterone and benign prostatic hyperplasia. Asian J Androl 2015 Mar-Apr;17(2):212-216. doi: 10.4103/1008-682X.140966.
- Shim JS, Kim JH, Yoon YS, Choi H, Park JY, Bae JH. Serum Testosterone Levels Are Negatively Correlated with International Prostate Symptom Score and Transitional Prostate Volume. Low Urin Tract Symptoms 2018 May;10(2):143-147. doi: 10.1111/luts.12150. Epub 2016 Nov 5.